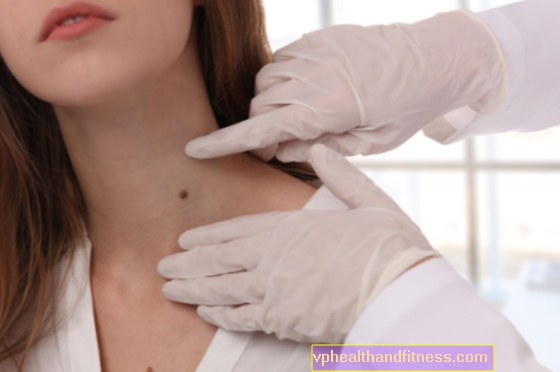
Torsdag 18. juli 2013.-En biologisk teknikk lot forskere fra National University (UN) i Colombia identifisere 200 menneskelige gener, i en skanning på 21 000, som kan være avgjørende for å utvikle mindre giftige og mer effektive behandlinger. Leishmaniasis er en sykdom forårsaket av veldig små parasitter (millioner av dem vil passe på tuppen av en pinne) som overføres under bitt av infiserte mygg (av slekten Lutzomyia).
Når de først er lokalisert i den indre delen av huden, angripes disse av en type hvite blodlegemer (spesialiserte celler som er en del av forsvarssystemet) kalt makrofager.
På tidspunktet for bittet "inntar" alt rundt seg sårene som patruljerer sårområdet. Dermed blir mange parasitter eliminert. Men andre overlever ikke bare, men kamuflerer seg for å komme inn i de samme cellene som angriper dem i live. Der forvandles de til å bli mer motstandsdyktige mot angrep.
Som en konsekvens begynner de å formere seg raskt i dem og infisere nye makrofager. Dermed spredte de seg i kroppen.
"Kroppen, i forsøk på å kontrollere infeksjonen og bli lurt av parasitter, klarer ikke bare å eliminere dem, men forårsaker skade på seg selv. Det er det vi kjenner som leishmaniasis, " forklarer Carlos Clavijo, lege i molekylær farmakologi og Toksikologi og professor ved National University of Colombia i Bogotá.
Ifølge eksperten, knyttet til Institutt for biologi, ved Det naturvitenskapelige fakultet, bedrar Leishmania (vitenskapelig navn på parasitten) makrofager og får dem til å avgi et slags overdrevet forsvarssignal, som er det som faktisk forårsaker sårene.
"De bruker forskjellige triks for å forvirre forsvarssystemet. Men vi tror at de trenger å bruke våre egne celler til det, " sier han. Gitt lærerens hypotese, er det mulig å utforme effektive metoder for å kontrollere dem hvis fellene de bruker er avklart.
Av denne grunn har Colciencias finansiert forskere i tre år ved FN og Federico Lleras Acosta Dermatological Institute som i fellesskap undersøker de involverte cellegener.
For å gjøre dette screenet forskerne 21 000 gener for å observere hvordan hver av dem forandret seg på grunn av Leishmania. Cellene som ble evaluert kom fra en cellelinje av kreftpasienter.
Parasitten interagerer med noen gener og manipulerer dem på en måte til å bruke dem til egen fordel. Makrofager fungerer som veldig komplekse maskiner, laget av tusenvis og tusenvis av små elementer (gener og proteiner), hvorav mange ikke vet nøyaktig hvordan de fungerer.
"Det vi gjorde var å sette opp et infisert makrofagsystem som ville tillate oss å studere funksjonen til genene av interesse, " sier professor Clavijo. For dette brukte de en biologisk teknikk som består i å slå dem av og på.
Verktøyet fungerer analogt med hvordan et kloks operativsystem blir evaluert. Hvis noen del fjernes, kan den fortsette å tjene. Ved å ta en annen, kan imidlertid noe mislykkes i driftssettet.
Ideen er da å installere og avinstallere komponentene, slik at du på denne måten kan bestemme hvilke deler som er viktige for at klokken skal fungere og hvilke som ikke er så mye. Forskere har valgt ut på en foreløpig måte 200 potensielt viktige gener som kan manipuleres.
Teknikken ble designet for å være forbigående: "Vi fjerner og setter inn hver komponent på nytt for å observere hvordan parasitten oppfører seg inne i makrofagen og dermed analyserer relevansen av disse mekanismene for den. Med verktøyet kan vi slå på eller av gener som vi ønsker og når vi vil ha det. "
Forskningen fokuserer på hvordan en makrofag fungerer og hvordan man bruker denne kunnskapen til å utvikle strategier for å kontrollere sykdommen.
"Mange av de kjente medikamentene fungerer ved å endre komponentene i cellene våre. Med de 200 genene kan vi artikulere informasjon om hvilke som er det viktigste som brukes av parasitten og hvilke medisiner som kan endre dem. Det er mulig at noen av disse har en positiv effekt på kontroll og derfor i behandlingen av sykdommen ", fremhever professor Clavijo.
Enda viktigere er at flertallet av arbeidet med sykdommen er konsentrert i studiet av parasitten, men det er ikke så mange studier som viser til makrofagen. Derfor peker undersøkelsen på sistnevnte. "Det vi leter etter er å få en mer effektiv og mindre giftig behandling, " sier forskeren.
Kilde:
Tags:
Diett-Og-Ernæring Familie Regenerering
Når de først er lokalisert i den indre delen av huden, angripes disse av en type hvite blodlegemer (spesialiserte celler som er en del av forsvarssystemet) kalt makrofager.
På tidspunktet for bittet "inntar" alt rundt seg sårene som patruljerer sårområdet. Dermed blir mange parasitter eliminert. Men andre overlever ikke bare, men kamuflerer seg for å komme inn i de samme cellene som angriper dem i live. Der forvandles de til å bli mer motstandsdyktige mot angrep.
Som en konsekvens begynner de å formere seg raskt i dem og infisere nye makrofager. Dermed spredte de seg i kroppen.
"Kroppen, i forsøk på å kontrollere infeksjonen og bli lurt av parasitter, klarer ikke bare å eliminere dem, men forårsaker skade på seg selv. Det er det vi kjenner som leishmaniasis, " forklarer Carlos Clavijo, lege i molekylær farmakologi og Toksikologi og professor ved National University of Colombia i Bogotá.
Ifølge eksperten, knyttet til Institutt for biologi, ved Det naturvitenskapelige fakultet, bedrar Leishmania (vitenskapelig navn på parasitten) makrofager og får dem til å avgi et slags overdrevet forsvarssignal, som er det som faktisk forårsaker sårene.
"De bruker forskjellige triks for å forvirre forsvarssystemet. Men vi tror at de trenger å bruke våre egne celler til det, " sier han. Gitt lærerens hypotese, er det mulig å utforme effektive metoder for å kontrollere dem hvis fellene de bruker er avklart.
Av denne grunn har Colciencias finansiert forskere i tre år ved FN og Federico Lleras Acosta Dermatological Institute som i fellesskap undersøker de involverte cellegener.
For å gjøre dette screenet forskerne 21 000 gener for å observere hvordan hver av dem forandret seg på grunn av Leishmania. Cellene som ble evaluert kom fra en cellelinje av kreftpasienter.
Parasitten interagerer med noen gener og manipulerer dem på en måte til å bruke dem til egen fordel. Makrofager fungerer som veldig komplekse maskiner, laget av tusenvis og tusenvis av små elementer (gener og proteiner), hvorav mange ikke vet nøyaktig hvordan de fungerer.
"Det vi gjorde var å sette opp et infisert makrofagsystem som ville tillate oss å studere funksjonen til genene av interesse, " sier professor Clavijo. For dette brukte de en biologisk teknikk som består i å slå dem av og på.
Verktøyet fungerer analogt med hvordan et kloks operativsystem blir evaluert. Hvis noen del fjernes, kan den fortsette å tjene. Ved å ta en annen, kan imidlertid noe mislykkes i driftssettet.
Ideen er da å installere og avinstallere komponentene, slik at du på denne måten kan bestemme hvilke deler som er viktige for at klokken skal fungere og hvilke som ikke er så mye. Forskere har valgt ut på en foreløpig måte 200 potensielt viktige gener som kan manipuleres.
Teknikken ble designet for å være forbigående: "Vi fjerner og setter inn hver komponent på nytt for å observere hvordan parasitten oppfører seg inne i makrofagen og dermed analyserer relevansen av disse mekanismene for den. Med verktøyet kan vi slå på eller av gener som vi ønsker og når vi vil ha det. "
Forskningen fokuserer på hvordan en makrofag fungerer og hvordan man bruker denne kunnskapen til å utvikle strategier for å kontrollere sykdommen.
"Mange av de kjente medikamentene fungerer ved å endre komponentene i cellene våre. Med de 200 genene kan vi artikulere informasjon om hvilke som er det viktigste som brukes av parasitten og hvilke medisiner som kan endre dem. Det er mulig at noen av disse har en positiv effekt på kontroll og derfor i behandlingen av sykdommen ", fremhever professor Clavijo.
Enda viktigere er at flertallet av arbeidet med sykdommen er konsentrert i studiet av parasitten, men det er ikke så mange studier som viser til makrofagen. Derfor peker undersøkelsen på sistnevnte. "Det vi leter etter er å få en mer effektiv og mindre giftig behandling, " sier forskeren.
Kilde:














-przyczyny-objawy-leczenie.jpg)


